琉球大学医学部 システム生理学講座|当教室は排尿生理に着目して、世界的な研究に取り組んでいます。
基礎研究
- トップページ
- 基礎研究
基礎研究
研究概要:宮里 実
排尿は、動物のマーキング、縄張り行動にみられるように、高次脳機能といった役割があります。一方で、生命の営みに必要不可欠な生命現象としての役割があります。加齢、生活習慣病、脳梗塞、パーキンソン病といった内科疾患、腹圧性尿失禁、骨盤臓器脱といった女性特有の疾患など、様々な原因で障害されます。基礎的手法、臨床で培ってきた知識と経験を生かして、橋渡し研究を追究しています。
宮里ラボの卒業生が、当基礎研究を共同研究者として支えています。
大城琢磨(那覇市立病院 泌尿器科、平成27年3月 大学院修了)
木村隆(琉球大学腎泌尿器外科、平成30年3月 大学院修了)
芦刈明日香(琉球大学腎泌尿器外科、平成31年3月 大学院修了)
大坪 亜紗斗 (長崎大学泌尿器科、令和3年3月 長崎大学大学院修了、当講座とのコラボで行った論文(Life Sci. 2021電子版))
長嶺覚子(システム生理、令和5年3月 大学院修了(Neurourol Urodyn. 2022掲載)
日下部直久(北海道大学泌尿器科、R3-4年特別研究学生(Int Urol Nephrol. 2023掲載)
川瀬紘太(岐阜大学泌尿器科。R4-5年特別研究学生)(Int Urol Nephrol. 2024掲載)
泉 恵一朗(琉球大学腎泌尿器科、令和7年6月 大学院修了)(Physiological Reports. 2025掲載)
排尿の中枢神経機構の解明
排尿には末梢神経だけではなく、仙髄、橋排尿中枢、大脳が関与するため、成熟という過程を経て構築されます。一日の大半は蓄尿であるため、中枢神経機構が制御の役割を果たします。このように、膀胱は、オン(排尿期)とオフ(蓄尿期)が存在する唯一の自律神経支配臓器です。私はこれまで、排尿の中枢神経機構の中で特に抑制系ニューロン(グリシン、GABA)の働きに着目して基礎研究を行ってきました。2004年~2006年米国のピッツバーグ大学泌尿器科に留学し、日本での研究をさらに発展させ、脊髄損傷ラットにヘルペスウイルスをvectorとしてGABAの産生酵素を遺伝子導入し、世界に先駆けて遠心路には影響せず、膀胱知覚(頻尿や膀胱痛)のみを改善させることを報告しました。難治性骨盤痛を標的とした新たな治療方法の開発を行っています。
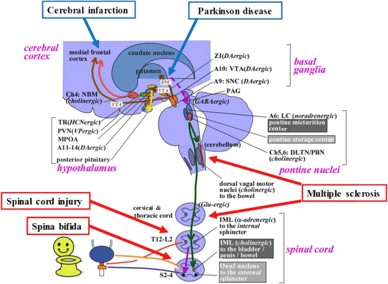
(Miyazato M et al. New Frontiers of Basic Science Research in Neurogenic Lower Urinary Tract Dysfunction. Urol Clin North Am. 2017 44(3):491-505.より抜粋)
膀胱機能の自然史に着目した排尿障害機序の解明
老化
膀胱も心臓のように生涯働く臓器であり、自然史が存在します。頻尿や尿意切迫を伴う過活動膀胱と残尿や尿閉に至る低活動膀胱は相反現象ではなく、過活動膀胱という代償機転がやがて不可逆的低活動膀胱に至る過程に着目しています。老齢ラットを用いて、加齢にともなう膀胱平滑筋細胞間結合蛋白(コネキシン43)の低下、膀胱虚血と線維化、一酸化窒素の分泌低下に伴う尿道弛緩反応の減弱を報告しました。加齢にともなう自律神経変化と排尿障害機序の解明を行っています。
糖尿病
糖尿病:糖尿病はその時間経過で膀胱機能にも悪影響を及ぼします。糖尿病ラットを用いた実験から、病初期は代償期で、高血糖による水分摂取の増加と尿量増加による一時的な頻尿を認めることが分かりました。中期には高血糖が神経終末へ作用することで膀胱収縮力が増強する一方で、収縮間隔が延び始めます。そして後期は非代償期に至り、残尿量が増え、排尿効率が低下するいわゆる低活動膀胱の病態を呈します。糖尿病中期までに治療介入を行うことで、糖尿病による膀胱障害の予後を改善する可能性があると考えます(Physiological Reports 2025)。
腹圧性尿失禁の発生機序と創薬の開発
腹圧性尿失禁の原因はこれまで解剖学的構築の破綻が原因とされてきましたが、これまでの私たちの基礎研究で脳幹を中心とする尿禁制反射の障害が主因であることが明らかとなりました。脳幹青斑核、縫線核からの下行経路に、尿禁制反射に関与するノルアドレナリン、セロトニン受容体が多く存在することを報告してきました。セロトニン2C受容体を標的とした創薬開発が私たちの研究をもとに始まっています。もう一つ別の経路として、オピオイド受容体の中でμ受容体が尿禁制反射を増強することを解明し、特許出願(特願2018-229643「脊髄オピオイドμ受容体を介した新規腹圧性尿失禁薬剤」)を行いました(宮里実、芦刈明日香)。脳梗塞(長嶺覚子、Neurourol Urodyn. 2022 41(8):1679-1691. doi: 10.1002/nau.25043) パーキンソン病モデル等を用いて腹圧性尿失禁の創薬の開発に取り組んでいます。
研究概要:上條 中庸
記憶は生命が生きていく上で欠かせないものです。海馬は記憶形成(覚えること)や想起(思い出すこと)に大きく関わっています。海馬の入り口に当たる歯状回では、外界からの空間情報や匂いなどの非空間情報の入力と脳内からの入力が統合されます。その情報統合が正常にできないとてんかんや鬱などが引き起こされることが知られています。そこで、電気生理学的手法を用いて海馬の特性を調べることによって記憶形成や疾患発生機序の神経基盤について解明する研究をしています。また、排尿と脳の関係について調べるために基礎研究と臨床研究の両方にに取り組みます。
海馬における記憶神経回路の解明
海馬は記憶が形成される部位として知られています。歯状回は様々な情報が初めに海馬への入力される入口です。外界からの五感で得られるような情報や脳内からの思考や集中の様なの情報が記憶をどのように形成するのかは分かっていません。私はこれまでに、歯状回の一つの神経細胞(入力を受ける樹状突起)で情報増強(入力情報が普通よりも大きくなる)ことや、神経細胞網(ニューラルネットワーク)にて外界からの異なる感覚情報が歯状回の入力する場所によって統合されやすくなることを報告してきました。今後、脳内からの情報がどの様に統合されるのかについて研究し、記憶形成の機序の解明を目指します。
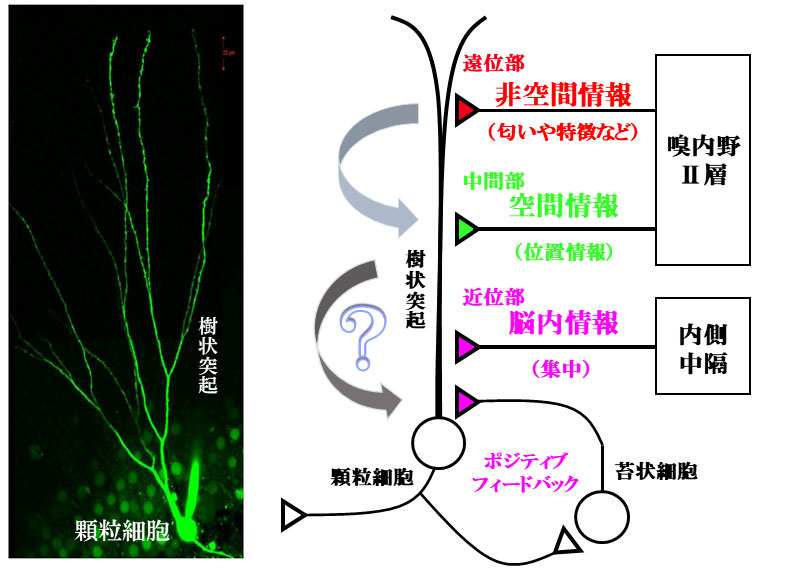
海馬における記憶形成神経回路の解明
海馬神経可塑性変化と下部尿路機能障害発生機序解明
ヒトは、成熟と学習により大脳に統合された自立した排尿機制御を獲得します。ネグレクトや虐待等の幼少期ストレスは、大脳機能に構造的変化を与え、排尿機能障害をもたらすことが知られています。例えば、心的外傷後ストレス障害(PTSD)は、夜尿・尿失禁等の排泄障害を誘発し社会適応に深刻な問題を引き起こしますが、有効な治療がありません。また、幼少期ストレスの一種である母子分離ストレスは幼少期だけではなく、成長後も排尿機能や行動にも影響することが分かりました(Kamijo & Miyazato, 2023)。近年、非侵襲的な対応策として神経可塑性を利用した治療方法が着目されています。そこで、幼若期のストレスが、脳の短期可塑性等障害をもたらし、さらに、ホルモン異常を引き起す結果、下部尿路機能障害を誘発する仮説を構築しました。ストレスによる脳、下部尿路機能障害の新たな疾患発症機序の解明を目指し、ホルモンバランスフィードバックと神経可塑性を利用した下部尿路機能障害治療・ストレス対策の確立を追求しています。
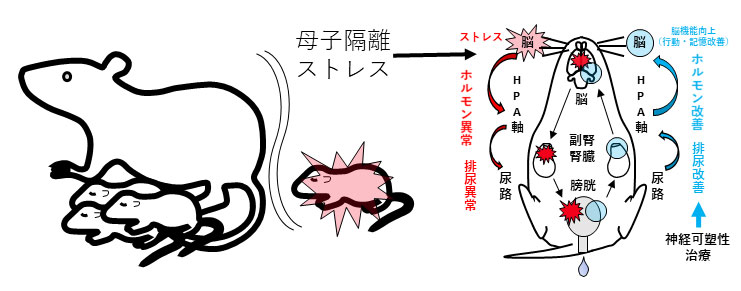
海馬神経可塑性変化と下部尿路機能障害発生機序解明
外尿道括約筋支配運動神経細胞へ投射される抑制入力の解明
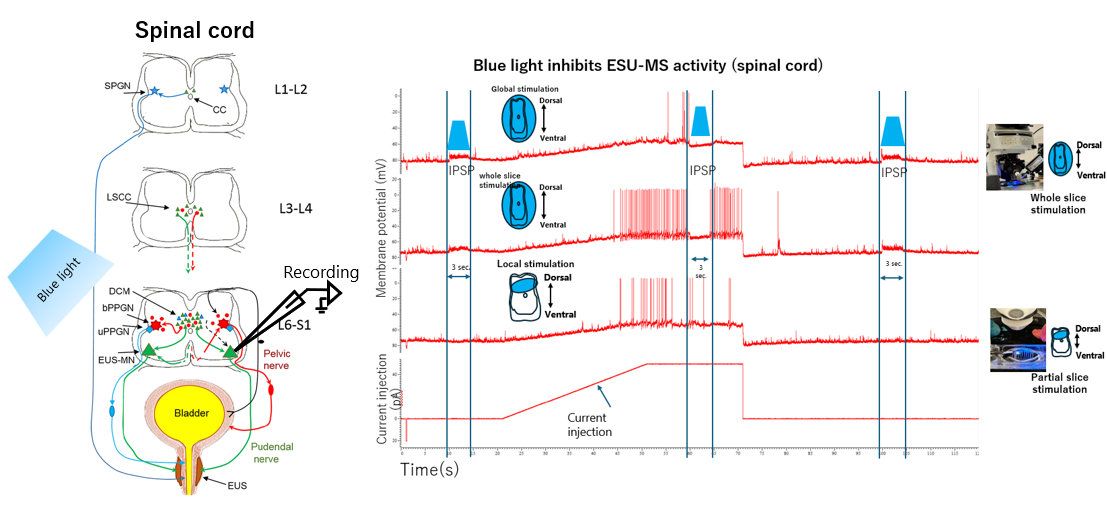
げっ歯類の正常な排尿には膀胱と外尿道括約筋の協調的制御が不可欠であり、これは脊髄Onuf核に存在する外尿道括約筋運動神経細胞(EUS-MN)への抑制性制御により実現されます。脊髄損傷等では、この抑制機能が破綻し排尿筋括約筋協調不全を引き起こしますが、その詳細なメカニズムは不明でした。
本研究では、革新的な斜め切片作製法を開発し、従来法では困難だった稀少なEUS-MNの効率的な記録を可能にしました。さらに、光遺伝学的手法とパッチクランプ記録を組み合わせ、EUS-MNへの抑制性入力の薬理学的特性を詳細に解析しました。
その結果、EUS-MNには時間特性の異なる2種類の抑制性応答(持続型・一過性)が存在し、持続型はグリシン・GABA両受容体、一過性は主にGABAA受容体により媒介されることを発見しました。この機能分化により、GABAergic伝達は急速な括約筋活動調節を、glycinergic伝達は排尿時の持続的括約筋弛緩を担うと考えられます。
これらの知見を基盤として、下部尿路制御に関わる脊髄局所神経回路の全容、特にEUS-MNのフィードバック回路解明を目指します。
研究者概要:https://researchmap.jp/chuyo
Email address:tadanobu@med.u-ryukyu.ac.jp
研究概要:黒部 匡広
年齢とともに、夜トイレに起きる、尿が近い、尿勢が弱い、漏れてしまうといった排尿・蓄尿にまつわる悩み事を持つ人が増えていきます。前立腺肥大症や過活動膀胱といった病気の背景には、前立腺や膀胱、尿道などの組織に様々な障害が生じています。様々な病態モデル動物を用いて、排尿・蓄尿障害の発生・進展のメカニズムを解明し、治療法の開発につなげる事を目指します。
過活動膀胱から低活動膀胱への進展メカニズムの解明
前立腺肥大症によって膀胱の出口が狭くなってくると、抵抗に打ち勝つために膀胱の平滑筋が肥大し、形態的・機能的な変化、いわゆる「リモデリング」が起こります。やがて膀胱の過剰な伸展や高圧環境によって虚血や神経の障害が生じ、頻尿や尿意切迫感といった過活動膀胱に特徴的な症状が出現します。その後、長期間リモデリングが進行すると、徐々に膀胱に線維組織が蓄積して収縮力が低下し、最終的には低活動膀胱、そして尿閉の状態へ移行します。私は2018年~2020年に米国のピッツバーグ大学泌尿器科に留学し、膀胱出口部閉塞モデルを用いて膀胱のリモデリングについての研究に取り組みました。引き続き研究を進展させ、新たな治療方法の開発を目指します。

尿道の各種受容体刺激と尿道括約筋の収縮
尿道は単に尿の通り道としての役割を担うのみならず、様々な受容体が発現し、膀胱頸部や尿道括約筋の収縮・弛緩に作用しています。興味深いことに尿道には旨味や苦味の受容体が存在する事も報告されています。また、腺細胞と神経細胞に共通する特性を持つ一群の内分泌・受容器細胞をパラニューロン細胞と呼びますが、その中でセロトニン分泌能を持つものが尿道に存在します。私はこれまで尿道におけるセロトニン陽性パラニューロンに着目し、セロトニン受容体と尿道括約筋の収縮反応への関与について研究を進めてきました。尿道括約筋の機能低下メカニズムを解明し、腹圧性尿失禁の新たな治療方法の開発を目指します。

尿道の各種受容体刺激による、尿道括約筋の収縮増強作用
